Përveç teknologjisë, sinteza e glikozideve ka qenë gjithmonë me interes për shkencën, pasi është një reaksion shumë i zakonshëm në natyrë. Punimet e fundit nga Schmidt, Toshima dhe Tatsuta, si dhe shumë referenca të cituara në to, kanë komentuar mbi një gamë të gjerë potencialesh sintetike.
Në sintezën e glikozideve, një përbërës shumësheqeror kombinohet me nukleofile, siç janë alkoolet, karbohidratet ose proteinat. Nëse kërkohet një reaksion selektiv me një nga grupet hidroksil të një karbohidrati, të gjitha funksionet e tjera duhet të mbrohen në hapin e parë. Në parim, proceset enzimatike ose mikrobike, për shkak të selektivitetit të tyre, mund të zëvendësojnë hapat kompleksë të mbrojtjes kimike dhe heqjes së mbrojtjes nga glikozidet në mënyrë selektive në rajone. Megjithatë, për shkak të historisë së gjatë të glikozideve alkil, zbatimi i enzimave në sintezën e glikozideve nuk është studiuar dhe zbatuar gjerësisht.
Për shkak të kapacitetit të sistemeve të përshtatshme enzimatike dhe kostove të larta të prodhimit, sinteza enzimatike e alkil poliglikozideve nuk është gati për t'u përmirësuar në nivelin industrial, dhe preferohen metodat kimike.
Në vitin 1870, MAcolley raportoi sintezën e "acetochlorhidrozës" (1, figura 2) me anë të reaksionit të dekstrozës (glukozës) me klorurin acetil, gjë që përfundimisht çoi në historinë e rrugëve të sintezës së glikozideve.
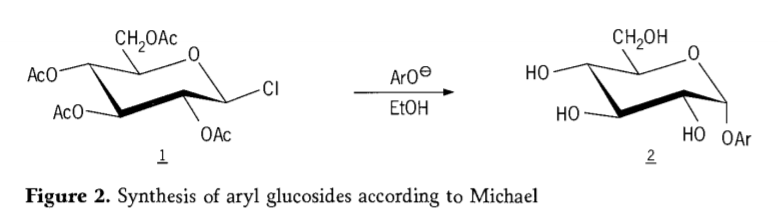
Halogjenurët tetra-0-acetil-glukopiranozil (acetohaloglukozat) u zbuluan më vonë se ishin ndërmjetës të dobishëm për sintezën stereoselektive të alkil glukozideve të pastra. Në vitin 1879, Arthur Michael arriti të përgatiste aril glikozide të përcaktuara dhe të kristalizueshme nga ndërmjetësit dhe fenolatet e Colley-t. (Aro-,Figura 2).
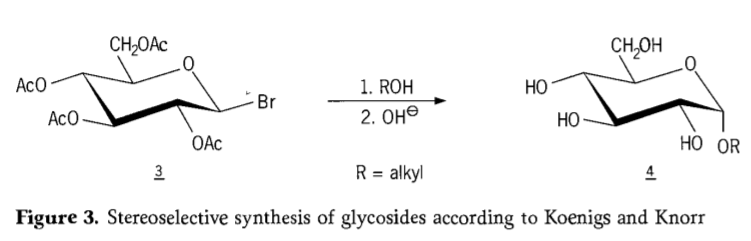
Në vitin 1901, sinteza e Michael në një gamë të gjerë karbohidratesh dhe aglikonesh hidroksilike, kur W. Koenigs dhe E. Knorr prezantuan procesin e tyre të përmirësuar të glikozidimit stereoselektiv (Figura 3). Reaksioni përfshin një zëvendësim SN2 në karbonin anomerik dhe vazhdon në mënyrë stereoselektive me përmbysje të konfigurimit, duke prodhuar për shembull α-glukozidin 4 nga β-anomeri i ndërmjetësit aceobromoglukozë 3. Sinteza Koenigs-Knorr zhvillohet në prani të promotorëve të argjendit ose merkurit.
Në vitin 1893, Emil Fischer propozoi një qasje thelbësisht të ndryshme për sintezën e glukozideve alkil. Ky proces tani njihet mirë si "glikozidimi i Fischer" dhe përfshin një reaksion të katalizuar nga acidi i glikozave me alkoolet. Sidoqoftë, çdo rrëfim historik duhet të përfshijë edhe përpjekjen e parë të raportuar të A. Gautier në vitin 1874, për të shndërruar dekstrozën me etanol anhidër në prani të acidit klorhidrik. Për shkak të një analize elementare mashtruese, Gautier besonte se kishte marrë një "diglukozë". Fischer më vonë demonstroi se "diglukoza" e Gautier ishte në fakt kryesisht etil glukozid (Figura 4).
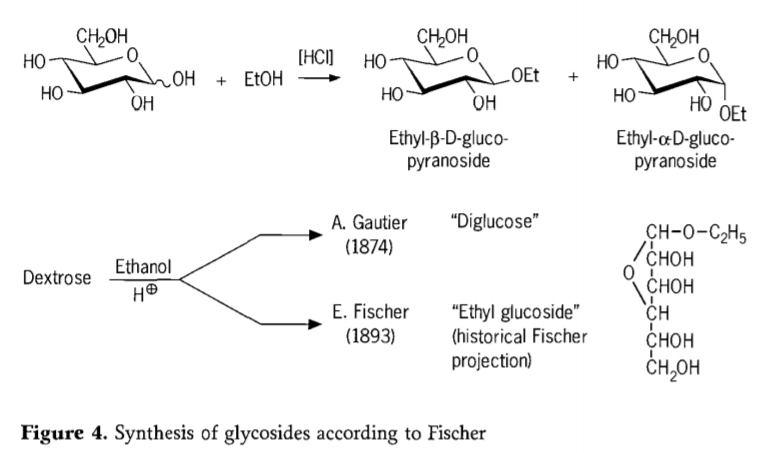
Fischer e përcaktoi saktë strukturën e etil glukozidit, siç mund të shihet nga formula historike furanozidike e propozuar. Në fakt, produktet e glikozidimit Fischer janë përzierje komplekse, kryesisht në ekuilibër të α/β-anomerëve dhe izomerëve piranozid/furanozid, të cilët gjithashtu përmbajnë oligomerë glikozidë të lidhur rastësisht.
Prandaj, speciet individuale molekulare nuk janë të lehta për t'u izoluar nga përzierjet e reaksionit Fischer, gjë që ka qenë një problem serioz në të kaluarën. Pas disa përmirësimeve të kësaj metode sinteze, Fischer më pas përvetësoi sintezën Koenigs-Knorr për hetimet e tij. Duke përdorur këtë proces, E. Fischer dhe B. Helferich ishin të parët që raportuan sintezën e një alkil glukozidi me zinxhir të gjatë që shfaqte veti surfaktante në vitin 1911.
Që në vitin 1893, Fischer kishte vënë re saktë vetitë thelbësore të alkilglikozideve, të tilla si stabiliteti i tyre i lartë ndaj oksidimit dhe hidrolizës, veçanërisht në mjedise fort alkaline. Të dyja karakteristikat janë të vlefshme për alkil poliglikozidet në aplikimet e surfaktantëve.
Hulumtimet në lidhje me reaksionin e glikozidimit janë ende në vazhdim dhe në të kaluarën e afërt janë zhvilluar disa rrugë interesante për glikozidet. Disa nga procedurat për sintezën e glikozideve janë përmbledhur në Figurën 5.
Në përgjithësi, proceset e glikozidimit kimik mund të ndahen në procese që çojnë në ekuilibra komplekse oligomerësh në shkëmbimin e glikozilit të katalizuar nga acidi.
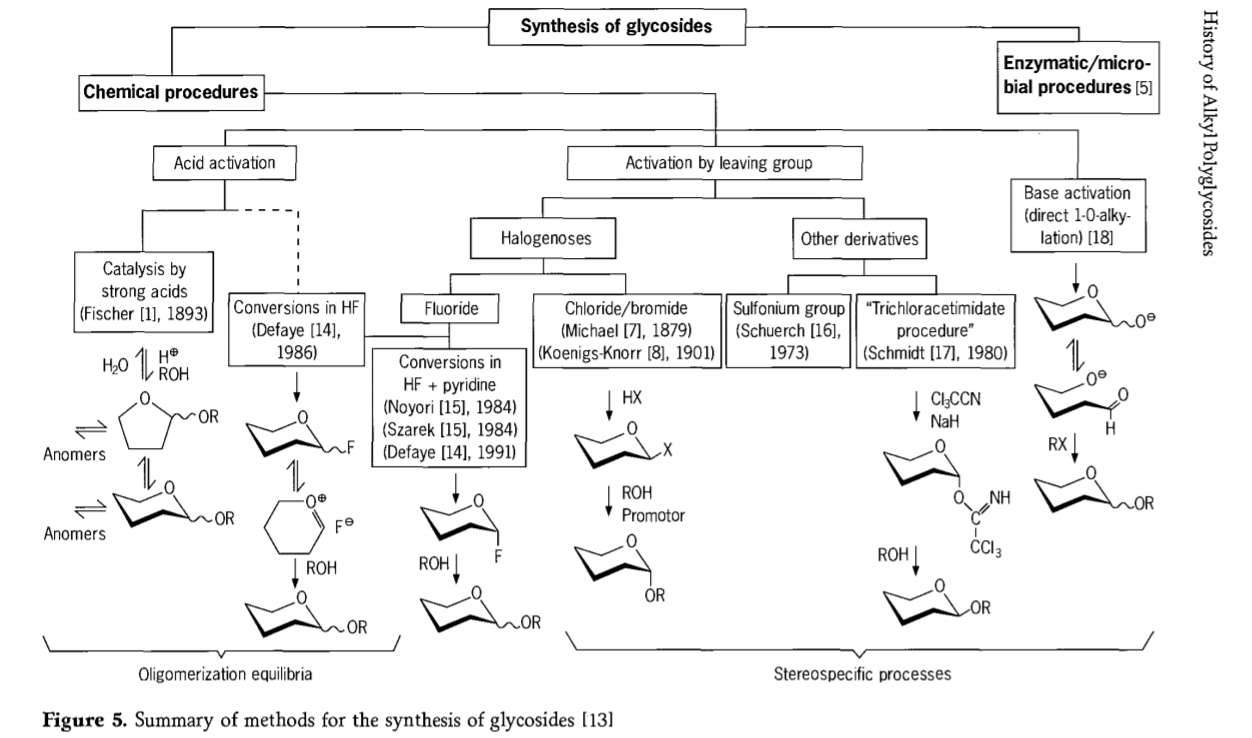
Reaksionet në substratet e karbohidrateve të aktivizuara në mënyrë të përshtatshme (reaksionet glikozidike Fischer dhe reaksionet e fluorurit të hidrogjenit (HF) me molekula karbohidratesh të pambrojtura) dhe reaksionet kinetike të kontrolluara, të pakthyeshme dhe kryesisht reaksionet e zëvendësimit stereotaksik. Një lloj i dytë procedure mund të çojë në formimin e specieve individuale në vend të përzierjeve komplekse të reaksioneve, veçanërisht kur kombinohet me teknikat e ruajtjes së grupeve. Karbohidratet mund të lënë grupe në karbonin ektopik, siç janë atomet e halogjenit, sulfonilet ose grupet trikloroacetimidate, ose të aktivizohen nga bazat para konvertimit në estere triflate.
Në rastin e veçantë të glikozidimeve në fluorur hidrogjeni ose në përzierjet e fluorur hidrogjeni dhe piridinës (piridinium poli [fluorur hidrogjeni]), fluoridet glikozil formohen in situ dhe shndërrohen pa probleme në glikozide, për shembull me alkoole. U tregua se fluorur hidrogjeni është një medium reagimi që aktivizohet fort dhe nuk degradohet; autokondensimi i ekuilibrit (oligomerizimi) vërehet i ngjashëm me procesin Fischer, megjithëse mekanizmi i reagimit është ndoshta i ndryshëm.
Glikozidet alkil kimikisht të pastra janë të përshtatshme vetëm për aplikime shumë të veçanta. Për shembull, glikozidet alkil janë përdorur me sukses në kërkimet biokimike për kristalizimin e proteinave të membranës, siç është kristalizimi tre-dimensional i porinës dhe bakterierodopsinës në prani të oktil β-D-glukopiranozidit (eksperimentet e mëtejshme bazuar në këtë punë çuan në çmimin Nobel në kimi për Deisenhofer, Huber dhe Michel në vitin 1988).
Gjatë zhvillimit të alkil poliglikozideve, metodat stereoselektive janë përdorur në shkallë laboratorike për të sintetizuar një sërë substancash model dhe për të studiuar vetitë e tyre fiziko-kimike. Për shkak të kompleksitetit të tyre, paqëndrueshmërisë së ndërmjetësve dhe sasisë dhe natyrës kritike të mbetjeve të procesit, sintezat e tipit Koenigs-Knorr dhe teknikat e tjera të grupeve mbrojtëse do të krijonin probleme të rëndësishme teknike dhe ekonomike. Proceset e tipit Fischer janë relativisht më pak të komplikuara dhe më të lehta për t'u kryer në shkallë komerciale dhe, në përputhje me rrethanat, janë metoda e preferuar për prodhimin e alkil poliglikozideve në shkallë të gjerë.
Koha e postimit: 12 shtator 2020





